Giải Hóa học 11 Kết nối bài 14 Ôn tập chương 3
56 tiết học trong chương trinh lớp 11 Kết Nối Tri Thức đều được Giaibaitapsgk tổng hợp qua những câu hỏi trắc nghiệm ngắn gọn. Các em có thể lựa chọn bộ câu hỏi tương ứng với từng tuần học để ôn tập kiến thức. Hơn nữa, các em học sinh có thể trực tiếp chọn câu trả lời và đối chiếu đáp án tự động ngay cuối trang siêu tiện lợi.
Giải bài 14: Ôn tập chương 3 sách Hóa học 11 Kết nối tri thức. Phần đáp án chuẩn, hướng dẫn giải chi tiết cho từng bài tập có trong chương trình học của sách giáo khoa. Hi vọng, các em học sinh hiểu và nắm vững kiến thức bài học.
I. HỆ THỐNG HÓA KIẾN THỨC
II. LUYỆN TẬP
Câu 1: Viết công thức cấu tạo các đồng phân mạch hở có cùng công thức phân tử C3H8O.
CH3-CH2-CH2-OH; CH3-CH(OH)-CH3; CH3-CH2-O-CH3.
Câu 2: Tại sao khi đun nóng đến nhiệt độ thích hợp, đường kính (màu trắng) chuyển thành màu nâu rồi màu đen?
Đường là hợp chất hữu cơ có công thức phân tử C12H22O11, khi đun nóng đến mức độ nhất định đường bị phân hủy, biến đổi thành hai chất là carbon (màu đen) và nước.
Câu 3: Hợp chất hữu cơ A có chứa carbon, hydrogen, oxygen, nitrogen. Thành phần phần trăm khối lượng của nguyên tố carbon, hydrogen, nitrogen lần lượt là 34,29%, 6,67%, 13,33%. Công thức phân tử của A cũng là công thức đơn giản nhất. Xác định công thức phân tử của A.
Gọi công thức phân tử của A là CxHyOzNt.
Ta có: x:y:z:t = 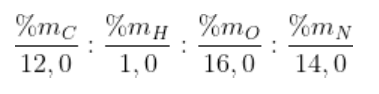 = 3:7:3:1
= 3:7:3:1
Công thức đơn giản nhất: C3H7O3N.
Công thức phân tử của A cũng là công thức đơn giản nhất.
Công thức phân tử của A là C3H7O3N.
Câu 4: Hợp chất A có công thức phân tử C3H6O. Khi đo phổ hồng ngoại cho kết quả như hình bên. Hãy xác định công thức cấu tạo của A.
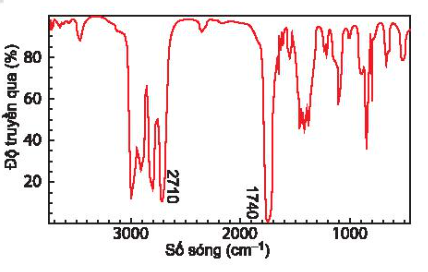
Công thức cấu tạo của A là CH3-CH2-CHO.
Nhóm chức có trong A là –CHO. Tín hiệu ở 1740 cm$^{-1}$ là tín hiệu dặc trưng của liên kết C═O, tín hiệu ở 2710 cm$^{-1}$ là các tín hiệu đặc trưng của liên kết C–H trong nhóm –CHO.
Câu 5: Retinol là một trong những thành phần chính tạo nên vitamin A có nguồn gốc động vật, có vai trò hỗ trợ thị giác của mắt, còn vitamin C giúp tăng khả năng miễn dịch của cơ thể. Để xác định công thức phân tử của các hợp chất này, người ta đã tiến hành phân tích nguyên tố và đo phổ khối lượng. Kết quả khảo sát được trình bày trong bảng sau:
| Hợp chất | % C | % H | % O | Giá trị m/z của peak ion phân tử [M$^{+}$] |
| Vitamin C | 40,90 | 4,55 | 54,55 | 176 |
| Vitamin A | 83,92 | 10,49 | 5,59 | 286 |
Hãy lập công thức phân tử của vitamin A và vitamin C.
Vitamin C:
Gọi công thức phân tử của vitamin C là CxHyOz.
Ta có: x:y:z = 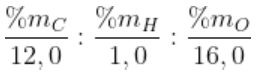 = p:q:r = 3:4:3
= p:q:r = 3:4:3
Công thức đơn giản nhất: C3H4O3
Phân tử khối của vitamin C là 88.
Mà CxHyOz = (CpHqOr)n $\Rightarrow $ 176 = 88.n $\Rightarrow $ n = 2
Công thức phân tử của vitamin C là C6H8O6.
Vitamin A:
Gọi công thức phân tử của vitamin A là CxHyOz.
Ta có: x:y:z = 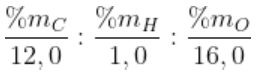 = p:q:r = 20:30:1
= p:q:r = 20:30:1
Công thức đơn giản nhất: C20H30O.
Phân tử khối của vitamin A là 286.
Mà CxHyOz = (CpHqOr)n $\Rightarrow $ 286 = 286.n $\Rightarrow $ n = 1
Công thức phân tử của vitamin A là C20H30O.
Đừng quên tham khảo tài liệu giải vở bài tập lớp 11 Kết Nối Tri Thức của Giaibaitapsgk. Dựa vào đó các em học sinh có thể nhanh chóng hoàn thành bài tập về nhà của mình.
Giaibaitapsgk cũng còn rất nhiều tài liệu học tốt siêu hay khác chờ các em khám phá: bộ đề thi Hoá học 11, ngân hàng câu hỏi trắc nghiệm 11, giải vở bài tập lớp 11 Kết Nối Tri Thức,... Hy vọng những tài liệu mà chúng tôi cung cấp sẽ giúp các em rút ngắn thời gian làm bài, giảm bớt áp lực học hành.
